Содержание
- 1 Михаил Мурашко о маркировке лекарственных средств, качестве препаратов и ценообразовании на медикаменты. Интервью газете «Известия»
- 2 Система маркировки лекарственных препаратов
- 3 Глава Росздравнадзора — о пользе введения маркировки лекарств и «контрольных закупках»
- 4 Как изменится работа медорганизаций с введением обязательной маркировки ЛП
- 5 МАРКИРОВКЕ ЛЕКАРСТВ НАШЛИ ПРОТИВОПОКАЗАНИЯ
- 6 Глава Росздравнадзора — о пользе введения маркировки лекарств и «контрольных закупках»
Счетчик обращений граждан и организаций
Михаил Мурашко о маркировке лекарственных средств, качестве препаратов и ценообразовании на медикаменты. Интервью газете «Известия»
«Контролировать аптеки сможет каждый потребитель самостоятельно»
Руководитель Росздравнадзора Михаил Мурашко — о маркировке лекарственных средств, качестве препаратов и ценообразовании на медикаменты
С 2019 года все производители лекарств будут обязаны маркировать свою продукцию специальными кодами. С помощью сканера в аптеке или программы на своем смартфоне покупатель сможет проверить происхождение упаковки и убедиться в легальности продукции. Эксперимент по маркировке лекарств стартовал, и с 1 июня в аптеках появятся аппараты для считывания информации. Отечественные производители лекарств уже заявили, что новация может стоить потребителям подорожания препаратов на 20%, а импортеры прогнозируют перебои с поставками. Руководитель Росздравнадзора Михаил Мурашко в эксклюзивном интервью корреспонденту «Известий» Элине Хетагуровой рассказал о своем видении влияния маркировки лекарств на их цену и о том, какую именно информацию смогут теперь получать потребители.
— В июне в аптеках появятся аппараты для считывания информации о лекарственном препарате. Как будет выглядеть метка и какую информацию получат потребители?
— Как и на каком этапе формируется информация о лекарственном препарате?
— Первые данные поступают в систему, как только происходит первая продажа с завода оптовику. Формируется облачная система, программа, в которую вносится информация от производителя, когда он выпускает в обращение данную упаковку, до конечного потребителя. Каждый участник цепочки передает свои данные. Производитель продал, дистрибьютор получил — каждый должен передать эти данные в систему. Благодаря этому можно отследить, где и у кого находится конкретная упаковка. В конце, когда пациент покупает препарат, сотрудники аптек списывают его из системы, но в самой системе всё равно останется информация о том, в какой именно аптеке купили медикамент. Таким образом, система еще и блокирует от возможного нелегального несанкционированного повторного ввода в обращение лекарства как в аптеке, так и в медицинских организациях.
— Как повлияет маркировка на качество медикаментов?
— Маркировка будет способствовать улучшению качества лекарственных препаратов. Понятно, что, если мы напечатаем на плохой препарат двухмерный код, он лучше от этого не станет. Именно поэтому государство создает систему маркировки как профилактическую, предупреждающую меру, позволяющую полностью исключить попадание недоброкачественных препаратов к потребителям. Во-первых, маркировка создаст условия для легальной цепи поставок, когда в аптечные сети попадают только те препараты, которые имеют понятное происхождение, вышли с официального завода. Нелегальные, непромаркированные препараты в сеть попасть не смогут. Это серьезная защита от вбросов. Но даже если в ходе надзорных мероприятий сотрудники Росздравнадзора выявят в аптеке некачественный препарат, то вся партия или серия данного лекарственного средства сразу же будет отозвана из оборота.
— Но препараты из одной партии или серии могут попасть в разные аптеки и даже разные регионы.
— Сегодня нам приходится писать письма с требованием к медицинским и аптечным организациям и территориальным органам проверить наличие недоброкачественного препарата и его изъятия в случае обнаружения. Это небыстрый процесс. Теперь же у нас будет возможность вывести бракованные лекарства из обращения нажатием одной кнопки. В программу вводится информация, мы сразу видим, какое количество препаратов и где находится в обращении из конкретной партии, при необходимости блокируем их, и каждый участник получает об этом факте информацию. После этого эти упаковки уже не смогут продавать, потому что система напишет, что они выведены из обращения.
— Как покупатели смогут получить информацию с метки на упаковке?
— Будет создано уникальное приложение для сканирования кодов, которое бесплатно скачивается в любой смартфон. С его помощью покупатели смогут считать всю информацию с кода.
— Но не у всех граждан есть смартфон, как получить необходимую информацию без него?
— В каждой аптеке обязательно будет установлено специальное оборудование, чтобы у пожилого человека или у тех, у кого нет смартфона, не возникло с этим никаких проблем. Подошел, поднес, отсканировал и убедился, что данный препарат является легальным и находится в обороте. Там будет вся та же самая информация, которая представлена в приложении для смартфонов. Разработка всей системы — это колоссальная трудоемкая работа. Территория России очень большая, и нужно сделать так, чтобы система работала и в онлайн-режиме, и офлайн, потому что в ряде регионов нестабильный интернет. Необходимо организовать работу так, чтобы была возможность выгружать данные пакетно — несколько раз в сутки или, например, через каждый час, для того чтобы у пациента всегда была возможность оперативно получить свежие данные. Все звенья должны работать четко, как часы. Права на ошибку мы не имеем, она может очень дорого стоить.
— То есть после того, как с 2019 года маркировка станет обязательной для всех производителей, на рынке не будет ни одного непромаркированного препарата?
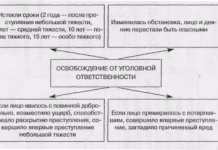
— Нет, те препараты, которые выпущены ранее, будут обращаться до истечения срока годности. В основном «срок жизни» препарата 1,5 года, то есть за это время препарат покупается точно. А срок годности максимально до пяти лет. Предполагается, что за 2–3 года все находящиеся в обращении препараты без маркировки будут куплены.
— Что грозит нарушителям, если все-таки будут найдены недоброкачественные или непромаркированные препараты, выпущенные после 2019 года?
— Маркировка исключает появление на рынке фальсификата и контрафакта?
— Да, поскольку это легальная цепь поставок. Если покупатели будут покупать лекарственные препараты только в лицензированных аптеках, то возможность попадания к ним фальсифицированного препарата исключается. Потому что, если, предположим, упаковку выпустили где-то на подпольном заводе, в аптеки ее ввести не смогут, она не попадет в систему, система не примет этот код, даже если вы сделаете какие-то фальсификации. Но если человек захочет найти приключение, купив препарат не в лицензированных аптеках или с рук, он его найдет, конечно. Но нужно ли ему шутить со своим здоровьем?
— Каково сегодня количество фальсификата и контрафакта на рынке лекарственных средств?
— Количество изымаемых из обращения недоброкачественных, фальсифицированных и контрафактных лекарственных средств составляет около 1% от всех серий лекарств, поступивших в обращение на российский рынок (около 250 тыс. серий). На фальсификат при этом приходится лишь 0,01%. Необходимо отметить, что легальный фармацевтический рынок стал значительно чище, чем это было 2–3 года назад. Уголовная ответственность заставляет быть честным и порядочным.
— Некоторые специалисты опасаются, что из-за маркировки хоть и улучшится качество и безопасность препаратов, но значительно повысится их стоимость, так как производителям и аптекам придется увеличить расходы на маркировку.
— Это не так. Есть разное оборудование для производства, для нанесения этих марок. Следовательно, разная цена. Она зависит от класса оборудования, его производительности: возможны решения и недорогие, и дорогостоящие. Допускается и напечатанный на упаковке код, и наклеенная саморазрушающаяся марка, которая может наклеиваться производителем, — это вообще недорогое решение. Она клеится на производственной линии так, что ее нельзя оторвать и переклеить. Если ее начать отрывать, она развалится. Это специальный стикер: клей и толщина бумаги, которая не позволяет переклеить с одной упаковки на другую. На сегодняшний день затраты на линию обходятся в пределах 2 млн рублей. Это чтобы полностью оснастить всю линию и полностью сделать всю систему маркировки. Это очень небольшие деньги в рамках всего производства, это даже в процентах не выражается никак. Это обычный принтер, срок работы которого до пяти лет. Дорогой вариант может стоить в пределах 6–7 млн рублей. Что тоже не так много. А сканер, который должен быть установлен в аптеках, хоть и будет за счет аптек, но он стоит в пределах 4–7 тыс. рублей. На одно рабочее место нужен один сканер.
— Позволит ли система маркировки прогнозировать дефицит того или иного препарата?
— База в единой системе поможет понять готовность региона, например, к подъему заболеваемости гриппом. То есть по системе можно будет понять, достаточно в регионе препаратов или нет. Спрогнозировать это, не имея такой информации, очень сложно. А так как теперь у нас будет информация о том, где и какое количество препаратов есть, а куда их необходимо отправить дополнительно, мы будем готовы к любой ситуации.
Система маркировки лекарственных препаратов
Счетчик обращений граждан и организаций
Система маркировки лекарственных препаратов
Глава Росздравнадзора — о пользе введения маркировки лекарств и «контрольных закупках»
ИНТЕРВЬЮ МИХАИЛА МУРАШКО АГЕНТСТВУ «ТАСС»
Несмотря на то, что некоторые производители жалуются на сложности, возникшие из-за введения маркировки, Михаил Мурашко отмечает, что подобная система действует во всех развитых странах
Когда покупатели смогут самостоятельно проверить легальность лекарств прямо в аптеке, почему через шесть лет на рынке не останется непромаркированных препаратов, почему регионы попадают под внеплановые проверки Росздравнадзора, кого коснется «контрольная закупка» и какие проблемы существуют в связи с тем, что граждане РФ безответственно относятся к своему здоровью, рассказал в интервью ТАСС глава Федеральной службы по надзору в сфере здравоохранения Михаил Мурашко.
— Михаил Альбертович, расскажите, пожалуйста, на каком этапе сейчас пилотный проект по маркировке лекарств. Некоторые производители говорят, что у них уже возникли сложности.
— Проект начался с тех производителей, у которых уже есть собственные наработки по маркировке, они создавали собственные системы. Основная задача сегодня состоит в том, чтобы состыковать систему предприятий с той глобальной системой, которая будет собирать информацию от всех производителей. Технические вопросы, формат обмена данными, согласование всех параметров передачи — это сейчас одна из самых актуальных и деликатных задач, которую необходимо решить. Нужно настроить все так, чтобы у производителей не возникало сбоев, потому что производство высокоскоростное, высокопоточное — задержки неприемлемы.
Еще один важный момент — оптовики. Мы в «пилоте» работаем с оптовыми организациями, которые имеют дело с максимальными объемами продукции. Поэтому важно, чтобы никаких сбоев на этапе формирования заказов и последующем перераспределении по аптекам не было.
— То есть сейчас, в принципе, проект идет в запланированном графике, если я правильно понимаю. Когда покупатель сможет самостоятельно оценить работу системы?
— Да, пилотный проект идет в запланированном графике. Уже в ближайшее время мы планируем совместно с налоговой службой продемонстрировать сами программные продукты и приложения, которые будут работать для покупателей.
Если говорить о том, какой объем данных будет доступен покупателю, то это однозначно будут данные о серии и о том, что она находится в легальном обороте (то есть что все процедуры по качеству и перемещениям легальны), срок годности, геопозиционирование. Вопрос по цене тоже решен — цена препарата будет передаваться в процессинговый центр. В дальнейшем мы планируем состыковать эту систему с реестром предельных отпускных цен. Финальный вариант будет доступен не сразу, но будем поэтапно вводить.
— Сколько сейчас в среднем занимает вывод недоброкачественного товара из оборота?
— Когда наши лаборатории выявляют проблемы по качеству серии, мы сразу же издаем письмо, в котором указываем серию препарата и производителя, который не прошел процедуру подтверждения качества, информируем все субъекты обращения лекарственного средства.
К сожалению, это не быстрый процесс, он может занять неделю, что в конечном итоге, конечно, не совсем эффективно в нашем быстро меняющемся мире. Именно система маркировки позволит оперативно отреагировать и сделать все необходимое одномоментно, в течение нескольких секунд: благодаря нажатию одной кнопки в программе, все участники рынка будут проинформированы и продажи данной серии или партии лекарственного препарата станут просто невозможными.
— К какому году тогда мы рассчитываем, что у нас непромаркированных лекарств не останется на рынке?
— Сегодня в проекте записано, что с 1 января 2019 года все вновь производимые препараты должны маркироваться. Средняя «продолжительность жизни» лекарства составляет где-то полтора-два года: до тех пор, пока оно не будет продано или отпущено в медицинскую организацию. Максимальные сроки годности лекарственных препаратов доходят до пяти лет. Исходя из этого, мы планируем, что после обязательного введения маркировки еще в течение пяти лет могут оставаться в обороте единичные непромаркированные фармпрепараты.
— А по стоимости препарата? Многие производители продолжают говорить о том, что маркировка повлияет на стоимость лекарств. Еще есть опасения, что зарубежные лекарства могут пропасть с российского рынка.
— Всегда нужно как можно больше говорить и объяснять, рождение слухов — это обычное явление. Маркировка вводится практически во всех развитых странах, все поняли ее преимущества, почувствовали ее вкус — и производители, и регуляторные органы, и пациенты. Сегодня в маркировке заинтересованы все. Поэтому для производителя — и отечественного, и зарубежного — это является, наоборот, преимуществом и комфортным вариантом, поскольку все рынки должны предъявлять единые требования. Мы же, в принципе, идем к тому, чтобы создавать условия для выхода отечественного производителя в том числе и на экспортные рынки. Производитель сам в этом заинтересован.
Жизнь показывает, что те, кто тянут до последнего момента, могут остаться не у дел. И понести убытки, именно из-за того, что они своевременно этого не сделали. В том, что касается стоимости: у производителя есть выбор, какую именно маркировку наносить на упаковку. Это может быть и печать на самой упаковке, и стикер. Мы находимся в тех же условиях, что и зарубежные страны, имеющие уже эту систему. Поэтому мы и наши партнеры не видим здесь никаких принципиальных — главное не затягивать и начать это делать уже сейчас.
— В РФ сейчас разрабатывается нормативная база для защиты прав социально уязвимых групп граждан, в число которых, например, попадают люди с инвалидностью. Ряд нормативов коснется лекарств в той части, где на упаковку будет необходимо наносить название шрифтом Брайля. Насколько это сейчас распространено?
— Ну для фармотрасли это не новшество. У нас это пока не повсеместно, но в рамках евразийского регулирования уже есть, и это нормальный процесс. Пока, к сожалению, это скорее эксклюзивная часть. В основном шрифт Брайля сегодня используют компании, которые поставляют свою продукцию одновременно на несколько рынков. Как только в России это станет обязательным условием, все производители к ним присоединятся.
— Давайте еще немного о регулировании. Контрольная закупка должна вступить в силу с июня. Кого коснется? Как повлияет на качество и доступность лекарств?
— Принятие нормативно-правового акта в июне маловероятно. Скорее — в осеннюю сессию. Контрольная закупка коснется всех субъектов, которые подпадают под контроль в обращении медицинской продукции, в том числе и медицинских услуг. В проекте сегодня это именно так рассматривается. Коснется, в первую очередь, лицензирования медицинской деятельности, рецептурного отпуска лекарств, выявления незарегистрированных медизделий. Это основная задача.
— Есть критерии оценки качества медицинской помощи, но при этом во многом результат, качество зависит от самого пациента приверженность к терапии, или здоровый образ жизни после операции на сердце. Как это сейчас учитывается?
— Проблема существует, и скрывать ее бессмысленно. Наглядный пример: один из пациентов в Красноярске имел тяжелую патологию сердечного клапана. В областной больнице ему сделали дорогостоящую операцию. В России эта операция вообще впервые выполнялась. Мы приезжаем в Красноярск, нам показали пациента, показали результаты операции, идем дальше знакомиться с работой медицинской организации и видим этого пациента уже на улице с сигаретой.
Понимаете, что произошло? Вся работа целой бригады врачей из-за курения пациента просто пошла насмарку. Поэтому мы всегда говорим о том, что необходима ответственность пациента за приверженность лечению. Работодатели это поняли давно, потому что им выгоден здоровый работник: они стимулируют отказ от курения, есть и другие программы. На уровне государства это тоже должно быть, но при этом не должны ущемляться основные права граждан и ограничиваться доступность медицинской помощи для них.
— А кто более ответственно относится к своему здоровью, мужчины или женщины?
— Если взять половую структуру населения, то до 35 лет количество мужчин и женщин фактически равное. А после 35 лет уже появляется разрыв. Для женщины нормально желание хорошо выглядеть, родить здорового ребенка, быть стройной. Поэтому у них здоровьесберегающее поведение больше выражено. У мужчин же оно, к сожалению, либо формируется позже, либо не успевает сформироваться, так как возникает хроническое заболевание. Поэтому необходима диспансеризация, необходима привычка следить за своим здоровьем, причем закладываться она должна в семье.
Есть такая шутка или анекдот, когда врача спросили: «Скажите, пожалуйста, как прожить дольше?» Он ответил: «Давайте исключим то, что сокращает жизнь». То есть вроде все просто, но как придерживаться, как избегать определенных искушений, которые сокращают жизнь и приносят какое-то временное удовольствие? Получить удовольствие от пробежки — это тоже хорошо.
— Если вернуться к теме нарушений, масса сообщений возникает каждый месяц в СМИ, о каких-то случаях врачебных ошибок и проверках. Чем заканчиваются такие истории?
— Мы публикуем отчеты о наших проверках, другое дело, что они занимают время, иногда недели или месяц, а срок жизни информации в интернете очень короткий. Если говорить о недавних случаях, например о том, который касался оказания стоматологической помощи девочке, то по нему уже завершена проверка и все материалы переданы в следственный комитет. Только в этом году мы уже три случая передали в следственные органы для дальнейшего расследования.
К большому сожалению, резонансные истории периодически случаются. Считаю, что «накала страстей» можно было бы избежать при грамотном общении медработника с пациентом или его родственниками. Все-таки, врачам необходимо даже тогда, когда наступил неблагоприятный исход, связанный с тяжелым течением заболевания и непредотвратимыми фатальными обстоятельствами, объяснять пациентам, объяснять их родственникам, почему это произошло. Необходимо уделять время этому объяснению.
Это общение для врача может быть тяжелым, но тем не менее и врачи, и пациенты, и журналисты, которые об этих историях пишут, должны понимать, что существуют сегодня состояния и заболевания или поздние обращения, когда действительно медики не в состоянии обеспечить сохранение жизни или сохранение здоровья.
— А по части проверок что делает Росздравнадзор?
— В таких случаях мы обязательно проводим проверки, как документарные, так и выездные. Мы запрашиваем информацию о внутреннем расследовании.
Сегодня сформировалась система внеплановых проверок по регионам. Она построена на рискоориентированных подходах — мы анализируем статистические показатели оперативной деятельности, которые позволяют нам принять решение, что этот регион в целом по оказанию медицинской помощи и по профилактическим направлениям, к сожалению, не добивается поставленных результатов, в том числе тех, которые прописаны в дорожных картах.
В этом году 12 таких регионов попали во внеплановые проверки в связи с тем, что показатели не соответствуют требованиям программы государственных гарантий и дорожным картам, например по медико-демографическим показателям снижения смертности или по использованию сердечно-сосудистой хирургии, тромболитической терапии, профилактическим мероприятиям, диспансеризации, лекарственному обеспечению и так далее. Когда мы видим, что по этим показателям регион не добивается результата, он тут же попадает в число регионов, подлежащих опеке.
— Не могу не вспомнить еще одну резонансную историю. Пару недель назад у нас депутат Милонов сделал предложение по регулированию товаров интимной сферы, в частности секс-игрушек. Должны ли они действительно быть лицензированы как медизделия?
— В Росздравнадзор обращение депутата не поступало, как не поступали и обращения граждан, связанные с безопасностью или в связи с какими-то осложнениями при применении этих изделий. Если в Службе появится официальный документ, то мы его рассмотрим в установленном законом порядке.
Как изменится работа медорганизаций с введением обязательной маркировки ЛП
В России продолжается эксперимент по внедрению системы маркировки лекарственных препаратов. Она станет обязательной с 1 января 2020 г., тогда все организации, имеющие лицензии на фармацевтическую и медицинскую деятельность, будут передавать данные в Федеральную государственную информационную систему «Мониторинг движения лекарственных препаратов» (МДЛП или ИС «Маркировка»). Для этого клиникам необходимо внедрить специальный электронный документооборот. Сделать это можно с помощью доработки существующей системы складского учета или установки дополнительного решения.
Общая характеристика системы МДЛП
Медучреждениям придется передавать информацию о получении ЛП от поставщика, их перемещении между отделениями, отпуске препаратов для медицинского применения, уничтожении и временном выводе из оборота. И если во время приемки препаратов информация о маркировке на упаковке и в системе мониторинга не совпадет, лекарства нужно будет возвращать поставщику. Закупать и применять ЛП, данные о которых не внесены в систему, запретят.
Перемещение препаратов должно отражаться в системе в течение 5 рабочих дней. Вероятно, после запуска системы в промышленную эксплуатацию срок будет сокращен до 1 рабочего дня.
ИС «Маркировка» – это электронный документооборот: принимаются только готовые документы, заверенные усиленной цифровой подписью. В ответ на загруженные данные приходит квитанция с положительным или отрицательным результатом. Поэтому к системе нельзя подключить сканнер штрих-кодов или формировать в ней документы о поступлении лекарств (они должны быть подготовлены во внешней системе). Требования к форме и содержанию описаны на официальном сайте оператора МДЛП в разделе «Маркировка лекарств» – «Документы» – «Разработчикам».
Способы организации обмена данными:
2) автоматически – по API.
Ручной вариант предполагает выгрузку документов с помощью личного кабинета на сайте и получение квитанций с результатом в ответ. При этом сами документы нужно готовить вне системы мониторинга. Интеграция по API позволяет организовать автоматический обмен.
Для регистрации на сайте потребуется усиленная цифровая подпись и данные из лицензии на медицинскую или фармацевтическую деятельность. Регистрация двухэтапная. Вначале нужно подтвердить, что организация – резидент РФ и авторизоваться с помощью электронной подписи. Затем откроется окно с заявлением.
ФИО руководителя и ИНН организации в цифровой подписи и в ЕГРЮЛ должны быть одинаковыми. Иначе для регистрации придется перевыпускать электронную подпись или вносить изменения в ЕГРЮЛ.
Срок рассмотрения заявления – 10 рабочих дней. Ответ придет на электронную почту. Статус заявления можно самостоятельно проверить на сайте системы. После подтверждения регистрации необходимо добавить пользователей и места оказания деятельности. Подробно процесс регистрации описан в Руководстве пользователя Личного кабинета.
Процесс выгрузки данных при получении лекарств от поставщика
Первая выгрузка данных в систему мониторинга должна произойти при получении лекарств от поставщика. Работа с ИС «Маркировка» предполагает заключение соглашения в свободной форме между поставщиком и клиникой об информационном обмене через систему. После заключения соглашения стороны добавляют друг друга в список доверенных контрагентов в личном кабинете системы. Заводить данные поставщика не нужно, он выбирается из готового реестра и появится в списке доверенных контрагентов после того, как подтвердит готовность к взаимодействию. Клиника может получить запрос на добавление и от поставщика.
| Видео (кликните для воспроизведения). |
Прямое и обратное акцептирование при приемке лекарств от поставщика
В информационном соглашении обязательно отражается, каким будет акцептирование: прямым или обратным. Загрузка документов с информацией о лекарствах и их передаче силами поставщика является прямым акцептированием. В этом случае клинике остается только подтвердить получение и согласиться с данными поставщика, либо инициировать процедуру возврата. Отсутствие входящего документа является обратным акцептированием. Это означает, что необходимо вносить информацию самостоятельно:
- заполнить реквизиты документа, включая данные о сроках годности, серии, контрольных идентификационных знаках и т.п.;
- отсканировать вторичную и транспортную упаковки.
После отправки документа, подготовленного самостоятельно, нужно получить подтверждение отгрузки от поставщика.
Согласно закону оба варианта равноправны. С точки зрения организации бизнес-процессов разработчики системы предпочтительным считают вариант прямого акцептирования. Скорее всего, именно он получит распространение.
При выгрузке данных в систему важно отслеживать результат регистрации документа в получаемой квитанции. Если он положительный, лекарства можно использовать. В противном случае нужно будет инициировать процесс возврата. Принять от поставщика можно и часть предложенной партии ЛП. Для этого нужно будет самостоятельно создать документ и получить подтверждение от контрагента.
Роль Регистратора выбытия
Второй раз клинике придется выгружать информацию во время использования препаратов или при их перемещении между отделениями. При использовании лекарств отправляемый в систему документ должен содержать указания на законодательные и/или установленные внутренними правилами основания для этого. В документе «Паспорта процессов, автоматизированные в ИС МДЛП» отражено, что можно выгружать информацию об использовании лекарств в первичной и вторичной упаковках. Но в рамках эксперимента маркируется только вторичная. Выгрузка информации о передаче лекарства для медицинского применения означает, что оно выбыло из оборота.
В требованиях к организации процесса выбытия прописано, что он должен проходить с обязательным применением специального прибора – «Регистратора выбытия». Речь о небольшом электронном устройстве с экраном, клавиатурой, встроенным сканером маркировки и несколькими разъемами для подключения к компьютеру или локальной сети. Работа с Регистратором начинается с создания накладной, акта списания или другого подобного документа со списком выбывающих препаратов. После создания документов нужно просканировать коды маркировки препаратов из списка. Подключение устройства к компьютеру позволяет сразу видеть результаты сканирования на экране. В противном случае сканирование происходит вслепую.
Для отправки информации в систему мониторинга с помощью Регистратора нужно еще внести номер и дату документа-основания выбытия. При интеграции устройства с информационной системой клиники вводить номера документов вручную не придется. Подключение Регистратора выбытия к локальной сети позволяет работать с ним сразу с нескольких компьютеров. При этом пользоваться встроенным сканером не получится. Вместо него можно будет использовать обычные сканеры штрих-кодов, подключенные к компьютеру. Но информация о выбытии будет отправляться с помощью Регистратора. Такой вариант подходит для крупных клиник и медицинских центров, так как у них, скорее всего, уже есть компьютеры и сканеры на рабочих местах.

Оператор системы должен предоставлять Регистратор выбытия за свой счет. Для получения устройства необходимо оформить запрос в разделе «Анкеты и договоры» личного кабинета. Перед оформлением запроса нужно ознакомиться с проектом договора на оснащение. После остается выбрать место деятельности, заполнить анкету на получение и дождаться результата ее рассмотрения.
Пока маркировка не станет обязательной, регистратор выдается только клиникам, которые участвуют в тестировании системы.
Противоречия в требованиях
С точки зрения частных клиник в требованиях к процессу выгрузки информации об использовании препаратов есть противоречие. Пациент получает препараты во время покупки медицинской услуги, продажа происходит через кассу, выписывается чек. Согласно требованиям, любой процесс продажи ЛП предполагает отправку данных в ИС «Маркировка» с помощью онлайн-кассы. То есть аналогично процессу передачи данных при розничных продажах в аптеках. Но такой вариант не подходит клиникам. Потому что для медицинского применения лекарства отгружаются в первичной упаковке или без нее. А передавать информацию пока возможно только о препаратах во вторичной упаковке. Как именно решится этот вопрос, скорее всего, выяснится только после 1 января 2020 г.
Перемещение препаратов внутри клиники
Процесс перемещения ЛП между складами или отделениями наиболее прост, так как информация уже загружена во время получения препаратов. Регистратор выбытия при этой процедуре тоже не используется. Достаточно подготовить документ-основание перемещения. Ошибки при выгрузке данных могут возникнуть, если информация о месте перемещения не указана в системе. При этом регистрировать можно только места, указанные в лицензии на медицинскую или фармацевтическую деятельность.
Для справки
Основная информация об обязательной маркировке ЛП располагается на портале «Честный знак» и официальном сайте Росздравнадзора. Там же можно найти ссылки на законодательные акты и постановления правительства.
Для тестирования механизмов взаимодействия медучреждений с ИС «Маркировка» созданы региональные Центры компетенций. Их список есть на сайте оператора системы. Московская ГКБ им. М.П. Кончаловского стала всероссийским Центром компетенции. На ее базе проводится обучение специалистов других медорганизаций. В специальном разделе на сайте больницы выложены материалы с описанием опыта взаимодействия с системой. Во многих материалах указано, что по различным вопросам можно обращаться на электронную почту начальника ИТ-отдела. Однако ответ можно получить только если клиника расположена в Москве и Московской области. Остальным придется обращаться в региональные Центры компетенции. При этом можно столкнуться с тем, что приказ о назначении такого центра не принят. Но в любом случае клиники из списка настраивали обмен с системой и скорее всего поделятся опытом.
Полезные документы
Текущие недоработки системы
Дублирование наименований лекарств
Работа в ИС «Маркировка» построена так, что одна из сторон соглашается с тем, какая информация ей передается. И возможности ее редактирования нет. При этом одинаковые лекарственные препараты в документах разных контрагентов могут называться по-разному. Это приводит к дублям в системе учета, от которых не избавиться. Когда появится единый реестр с названиями препаратов, неизвестно.
Передача информации о выводе лекарств из оборота раньше их использования
Маркировка только вторичной упаковки привела к тому, что при отгрузке ЛП для медицинского применения в систему мониторинга выгружается информация только о ней. То есть препараты выводятся из оборота раньше, чем могут быть израсходованы. Поэтому возникают ситуации, когда по законным причинам лекарства могут быть не израсходованы, но выведены из оборота. Механизм обратного ввода в оборот существует. Но в случае с медорганизациями пока не понятно, что является достаточным основанием для этого.
Брак при нанесении штрихкодов с криптозащитой
Есть нерешенные проблемы и на этапе упаковки препаратов. Фармпроизводители утверждают, что при нанесении штрихкодов с криптозащитой, процент брака доходит до 89%. Связано это с длиной электронной подписи. По действующим нормативным актам она должна состоять из 88 знаков. Производители просят ее сократить до 20. Вопрос пока не решен, однако переносить сроки внедрения обязательной маркировки не планируется.
Согласно постановлению Правительства РФ от 14.12.2018 г. № 1557, субъекты обращения лекарственных средств из перечня высокозатратных нозологий обязаны зарегистрироваться в ИС «Маркировка» в период с 1 июля по 8 июля 2019 г. После регистрации есть 21 календарный день на подготовку к информационному взаимодействию с системой и оформление заявки для участия в тестировании, которое продлится 2 месяца.
Наказание за нарушения
Согласно подготовленным изменениям в Кодекс об административных правонарушениях РФ, за несвоевременное внесение данных в систему мониторинга, либо внесение в нее недостоверной информации с 1 января 2020 г. будет грозить штраф для должностных лиц в размере от 5 тыс. до 10 тыс. руб., для юрлиц – от 50 до 100 тыс. руб. Составлять протоколы и рассматривать дела будет Росздравнадзор.
Что делать медицинским организациям
Выгрузка документов в ИС «Маркировка» возможна только при использовании внешней системы для их формирования. Это можно сделать в медицинской информационной системе (МИС) или в отдельном решении для складского учета. Обмен данными через МИС возможен при наличии нужной функциональности. Если клиника уже работает с МИС, то внедрение отдельного решения усложнит учет и увеличит нагрузку на персонал. Доработка МИС будет более эффективным решением. Финансовая сторона доработки зависит от системы, с которой работает клиника.
Установка отдельной системы для учета – рабочий вариант для медорганизаций, которые не используют МИС. Правда, при условии, что установка МИС не планируется. Если система для складского учета разработана самостоятельно, логично будет сопоставить бюджет доработки со стоимостью готовых продуктов на рынке.
Материал подготовлен МИС «МедАнгел».
Самые важные новости сферы здравоохранения теперь и в нашем Telegram-канале @medpharm.
МАРКИРОВКЕ ЛЕКАРСТВ НАШЛИ ПРОТИВОПОКАЗАНИЯ
Фармрынку пообещали продлить реформу.
Минпромторг неожиданно пошел навстречу представителям фарминдустрии, пообещав продлить сроки введения обязательной маркировки лекарств. Нынешняя версия реформы предполагает, что к 1 января 2019 г. в обороте не останется немаркированных препаратов. По мнению же участников рынка, такие темпы разрушат отечественную фармацевтику непомерными тратами и повысят цены на препараты.
Как заявила в ходе круглого стола в Госдуме заместитель главы департамента развития фармацевтической промышленности Минпромторга Елена Денисова, министерство готово пересмотреть сроки введения маркировки лекарств в РФ. Напомним, 1 февраля начат добровольный эксперимент по их маркировке, оператором системы является ФНС. По поправкам к закону «Об обращении лекарственных средств», охват всех лекарств в обороте должен быть завершен к 31 декабря 2018 года.
Как рассказал в ходе мероприятия заместитель главы ФНС Андрей Батуркин, уже промаркировано 1,9 млн упаковок, в пилотном проекте участвуют 310 компаний, в системе зарегистрирован 41 препарат. Кроме того, готово мобильное приложение, с помощью которого потребитель может проверить, есть ли купленное лекарство в системе маркировки. В самом Минпромторге “Ъ” вчера пояснили, что перенос сроков могут рассмотреть для конкретных групп препаратов после анализа «технологической готовности» производителей к развертыванию системы мониторинга движения лекарств.
Источник “Ъ” в правительстве говорит, что необходимость отсрочки очевидна, «такие проекты за год сложно реализовать, международный опыт показывает, что в разных странах этот процесс занимал два-три года». По его словам, корректно было бы обязать к маркировке в 2018 году только производителей дорогостоящих препаратов, входящих в программу «Семь нозологий», их всего пятьдесят, и это не создаст пиковой нагрузки на систему.
Представители компании Stada CIS предлагают сдвинуть ввод маркировки на два года: в 2019-м начать внедрение системы для дорогостоящих препаратов, участвующих в госзакупках, а с 2021 года погрузить в нее все остальные. Заместитель главы компании Иван Глушков рассказал “Ъ”, что на заседании глава Росздравнадзора Михаил Мурашко впервые официально заявил о готовности рассмотреть варианты продления сроков, хотя согласия с конкретными предложениями не выражал. Отказа от маркировки дешевых препаратов, о чем просят их производители, глава ведомства категорически не поддерживает. В ответ на это Борис Шпигель, владелец ГК «Биотэк», одного из производителей дешевых лекарств, заявил, что это «последний этап разрушения отечественной фармацевтики, которое началось в 2010 году».
Совладелец фармзавода «Озон» (Самарская область, производит препараты средней стоимостью до 20 руб.) Виталий Алейников считает, что «пилот» по маркировке необходимо продлить до 2018 года, и тогда уже определить сроки тотального ее внедрения. «Но инициаторы проекта не согласны»,— добавил он. Господин Алейников рассказал, что в случае перехода на маркировку с 2018 года стоимость лекарств «Озона» вырастет примерно на 15%. «Часть нашей продукции — ЖНВЛП (жизненно необходимые и важнейшие лекарственные препараты.— “Ъ”), стоимость которых регулируется, нам придется отказаться от производства примерно 100 млн упаковок (треть выпуска), и эти лекарства будут замещены более дорогими аналогами»,— резюмировал он.
Участники круглого стола высказывали опасения и в связи с передачей системы маркировки структурам «Ростеха», но, согласно протоколу совещания правительства по маркировке от 10 ноября (есть у “Ъ”), проект маркировки лекарств будет единственным, который в ведение госкорпорации не отойдет.
Счетчик обращений граждан и организаций
Глава Росздравнадзора — о пользе введения маркировки лекарств и «контрольных закупках»
ИНТЕРВЬЮ МИХАИЛА МУРАШКО АГЕНТСТВУ «ТАСС»
Несмотря на то, что некоторые производители жалуются на сложности, возникшие из-за введения маркировки, Михаил Мурашко отмечает, что подобная система действует во всех развитых странах
Когда покупатели смогут самостоятельно проверить легальность лекарств прямо в аптеке, почему через шесть лет на рынке не останется непромаркированных препаратов, почему регионы попадают под внеплановые проверки Росздравнадзора, кого коснется «контрольная закупка» и какие проблемы существуют в связи с тем, что граждане РФ безответственно относятся к своему здоровью, рассказал в интервью ТАСС глава Федеральной службы по надзору в сфере здравоохранения Михаил Мурашко.
— Михаил Альбертович, расскажите, пожалуйста, на каком этапе сейчас пилотный проект по маркировке лекарств. Некоторые производители говорят, что у них уже возникли сложности.
— Проект начался с тех производителей, у которых уже есть собственные наработки по маркировке, они создавали собственные системы. Основная задача сегодня состоит в том, чтобы состыковать систему предприятий с той глобальной системой, которая будет собирать информацию от всех производителей. Технические вопросы, формат обмена данными, согласование всех параметров передачи — это сейчас одна из самых актуальных и деликатных задач, которую необходимо решить. Нужно настроить все так, чтобы у производителей не возникало сбоев, потому что производство высокоскоростное, высокопоточное — задержки неприемлемы.
Еще один важный момент — оптовики. Мы в «пилоте» работаем с оптовыми организациями, которые имеют дело с максимальными объемами продукции. Поэтому важно, чтобы никаких сбоев на этапе формирования заказов и последующем перераспределении по аптекам не было.
— То есть сейчас, в принципе, проект идет в запланированном графике, если я правильно понимаю. Когда покупатель сможет самостоятельно оценить работу системы?
— Да, пилотный проект идет в запланированном графике. Уже в ближайшее время мы планируем совместно с налоговой службой продемонстрировать сами программные продукты и приложения, которые будут работать для покупателей.
Если говорить о том, какой объем данных будет доступен покупателю, то это однозначно будут данные о серии и о том, что она находится в легальном обороте (то есть что все процедуры по качеству и перемещениям легальны), срок годности, геопозиционирование. Вопрос по цене тоже решен — цена препарата будет передаваться в процессинговый центр. В дальнейшем мы планируем состыковать эту систему с реестром предельных отпускных цен. Финальный вариант будет доступен не сразу, но будем поэтапно вводить.
— Сколько сейчас в среднем занимает вывод недоброкачественного товара из оборота?
— Когда наши лаборатории выявляют проблемы по качеству серии, мы сразу же издаем письмо, в котором указываем серию препарата и производителя, который не прошел процедуру подтверждения качества, информируем все субъекты обращения лекарственного средства.
К сожалению, это не быстрый процесс, он может занять неделю, что в конечном итоге, конечно, не совсем эффективно в нашем быстро меняющемся мире. Именно система маркировки позволит оперативно отреагировать и сделать все необходимое одномоментно, в течение нескольких секунд: благодаря нажатию одной кнопки в программе, все участники рынка будут проинформированы и продажи данной серии или партии лекарственного препарата станут просто невозможными.
— К какому году тогда мы рассчитываем, что у нас непромаркированных лекарств не останется на рынке?
— Сегодня в проекте записано, что с 1 января 2019 года все вновь производимые препараты должны маркироваться. Средняя «продолжительность жизни» лекарства составляет где-то полтора-два года: до тех пор, пока оно не будет продано или отпущено в медицинскую организацию. Максимальные сроки годности лекарственных препаратов доходят до пяти лет. Исходя из этого, мы планируем, что после обязательного введения маркировки еще в течение пяти лет могут оставаться в обороте единичные непромаркированные фармпрепараты.
— А по стоимости препарата? Многие производители продолжают говорить о том, что маркировка повлияет на стоимость лекарств. Еще есть опасения, что зарубежные лекарства могут пропасть с российского рынка.
— Всегда нужно как можно больше говорить и объяснять, рождение слухов — это обычное явление. Маркировка вводится практически во всех развитых странах, все поняли ее преимущества, почувствовали ее вкус — и производители, и регуляторные органы, и пациенты. Сегодня в маркировке заинтересованы все. Поэтому для производителя — и отечественного, и зарубежного — это является, наоборот, преимуществом и комфортным вариантом, поскольку все рынки должны предъявлять единые требования. Мы же, в принципе, идем к тому, чтобы создавать условия для выхода отечественного производителя в том числе и на экспортные рынки. Производитель сам в этом заинтересован.
Жизнь показывает, что те, кто тянут до последнего момента, могут остаться не у дел. И понести убытки, именно из-за того, что они своевременно этого не сделали. В том, что касается стоимости: у производителя есть выбор, какую именно маркировку наносить на упаковку. Это может быть и печать на самой упаковке, и стикер. Мы находимся в тех же условиях, что и зарубежные страны, имеющие уже эту систему. Поэтому мы и наши партнеры не видим здесь никаких принципиальных — главное не затягивать и начать это делать уже сейчас.
— В РФ сейчас разрабатывается нормативная база для защиты прав социально уязвимых групп граждан, в число которых, например, попадают люди с инвалидностью. Ряд нормативов коснется лекарств в той части, где на упаковку будет необходимо наносить название шрифтом Брайля. Насколько это сейчас распространено?
— Ну для фармотрасли это не новшество. У нас это пока не повсеместно, но в рамках евразийского регулирования уже есть, и это нормальный процесс. Пока, к сожалению, это скорее эксклюзивная часть. В основном шрифт Брайля сегодня используют компании, которые поставляют свою продукцию одновременно на несколько рынков. Как только в России это станет обязательным условием, все производители к ним присоединятся.
— Давайте еще немного о регулировании. Контрольная закупка должна вступить в силу с июня. Кого коснется? Как повлияет на качество и доступность лекарств?
— Принятие нормативно-правового акта в июне маловероятно. Скорее — в осеннюю сессию. Контрольная закупка коснется всех субъектов, которые подпадают под контроль в обращении медицинской продукции, в том числе и медицинских услуг. В проекте сегодня это именно так рассматривается. Коснется, в первую очередь, лицензирования медицинской деятельности, рецептурного отпуска лекарств, выявления незарегистрированных медизделий. Это основная задача.
— Есть критерии оценки качества медицинской помощи, но при этом во многом результат, качество зависит от самого пациента приверженность к терапии, или здоровый образ жизни после операции на сердце. Как это сейчас учитывается?
— Проблема существует, и скрывать ее бессмысленно. Наглядный пример: один из пациентов в Красноярске имел тяжелую патологию сердечного клапана. В областной больнице ему сделали дорогостоящую операцию. В России эта операция вообще впервые выполнялась. Мы приезжаем в Красноярск, нам показали пациента, показали результаты операции, идем дальше знакомиться с работой медицинской организации и видим этого пациента уже на улице с сигаретой.
Понимаете, что произошло? Вся работа целой бригады врачей из-за курения пациента просто пошла насмарку. Поэтому мы всегда говорим о том, что необходима ответственность пациента за приверженность лечению. Работодатели это поняли давно, потому что им выгоден здоровый работник: они стимулируют отказ от курения, есть и другие программы. На уровне государства это тоже должно быть, но при этом не должны ущемляться основные права граждан и ограничиваться доступность медицинской помощи для них.
— А кто более ответственно относится к своему здоровью, мужчины или женщины?
— Если взять половую структуру населения, то до 35 лет количество мужчин и женщин фактически равное. А после 35 лет уже появляется разрыв. Для женщины нормально желание хорошо выглядеть, родить здорового ребенка, быть стройной. Поэтому у них здоровьесберегающее поведение больше выражено. У мужчин же оно, к сожалению, либо формируется позже, либо не успевает сформироваться, так как возникает хроническое заболевание. Поэтому необходима диспансеризация, необходима привычка следить за своим здоровьем, причем закладываться она должна в семье.
Есть такая шутка или анекдот, когда врача спросили: «Скажите, пожалуйста, как прожить дольше?» Он ответил: «Давайте исключим то, что сокращает жизнь». То есть вроде все просто, но как придерживаться, как избегать определенных искушений, которые сокращают жизнь и приносят какое-то временное удовольствие? Получить удовольствие от пробежки — это тоже хорошо.
— Если вернуться к теме нарушений, масса сообщений возникает каждый месяц в СМИ, о каких-то случаях врачебных ошибок и проверках. Чем заканчиваются такие истории?
— Мы публикуем отчеты о наших проверках, другое дело, что они занимают время, иногда недели или месяц, а срок жизни информации в интернете очень короткий. Если говорить о недавних случаях, например о том, который касался оказания стоматологической помощи девочке, то по нему уже завершена проверка и все материалы переданы в следственный комитет. Только в этом году мы уже три случая передали в следственные органы для дальнейшего расследования.
К большому сожалению, резонансные истории периодически случаются. Считаю, что «накала страстей» можно было бы избежать при грамотном общении медработника с пациентом или его родственниками. Все-таки, врачам необходимо даже тогда, когда наступил неблагоприятный исход, связанный с тяжелым течением заболевания и непредотвратимыми фатальными обстоятельствами, объяснять пациентам, объяснять их родственникам, почему это произошло. Необходимо уделять время этому объяснению.
Это общение для врача может быть тяжелым, но тем не менее и врачи, и пациенты, и журналисты, которые об этих историях пишут, должны понимать, что существуют сегодня состояния и заболевания или поздние обращения, когда действительно медики не в состоянии обеспечить сохранение жизни или сохранение здоровья.
— А по части проверок что делает Росздравнадзор?
— В таких случаях мы обязательно проводим проверки, как документарные, так и выездные. Мы запрашиваем информацию о внутреннем расследовании.
Сегодня сформировалась система внеплановых проверок по регионам. Она построена на рискоориентированных подходах — мы анализируем статистические показатели оперативной деятельности, которые позволяют нам принять решение, что этот регион в целом по оказанию медицинской помощи и по профилактическим направлениям, к сожалению, не добивается поставленных результатов, в том числе тех, которые прописаны в дорожных картах.
В этом году 12 таких регионов попали во внеплановые проверки в связи с тем, что показатели не соответствуют требованиям программы государственных гарантий и дорожным картам, например по медико-демографическим показателям снижения смертности или по использованию сердечно-сосудистой хирургии, тромболитической терапии, профилактическим мероприятиям, диспансеризации, лекарственному обеспечению и так далее. Когда мы видим, что по этим показателям регион не добивается результата, он тут же попадает в число регионов, подлежащих опеке.
— Не могу не вспомнить еще одну резонансную историю. Пару недель назад у нас депутат Милонов сделал предложение по регулированию товаров интимной сферы, в частности секс-игрушек. Должны ли они действительно быть лицензированы как медизделия?
| Видео (кликните для воспроизведения). |
— В Росздравнадзор обращение депутата не поступало, как не поступали и обращения граждан, связанные с безопасностью или в связи с какими-то осложнениями при применении этих изделий. Если в Службе появится официальный документ, то мы его рассмотрим в установленном законом порядке.
Источники
Молчанов, В.И. Огнестрельные повреждения и их судебно-медицинская экспертиза: Руководство для врачей / В.И. Молчанов, В.Л. Попов, К.Н. Калмыков. — М.: Медицина, 2014. — 272 c.
Гойко, Л.Ф. Судебные были; К.: Украина, 2012. — 208 c.
Жмудь, Л. Я. Зарождение истории науки в античности / Л.Я. Жмудь. — М.: Издательство Русского Христианского Гуманитарного Института, 2017. — 424 c.

Имею высшее образование по специальности: юрист по финансово-правовому профилю. Мой стаж работы в юридической компании составляет 12 лет. Очень рад Вас видеть на своем сайте!